
| Российский химико-аналитический портал | ::: портал химиков-аналитиков ::: химический анализ и аналитическая химия в фокусе внимания ::: |
 |
|
| ANCHEM.RU » Литература » Справочные, учебные материалы / книги » ... |
Комментарий ANCHEM.RU: Данный материал не претендует на полноту изложения, сопоставимую с научными обзорами и учебниками, и предназначен скорее для ознакомительного прочтения. Приветствуется дополнение и уточнение деталей другими авторами.
В последние 30-40 лет наши знания о химической природе жизни растений и животных, и окружающего нас физического мира чрезвычайно возросли благодаря аналитическим возможностям мощных приборов. Чувствительность широко используемых современных методов так высока, что количество вещества в 1мкг, столь малое, что его нельзя увидеть глазом, может быть легко зарегистрировано и идентифицировано. Все эти инструментальные методы основаны на относительно хорошо известных и довольно простых физических и химических законах.
Большинство анализируемых образцов представляют собой смеси. Даже при использовании эффективных способов пробоподготовки для выделения интересующих соединений анализировать все же приходится смесь. Значение газовой и жидкостной хроматографии объясняется их способностью разделять компоненты смеси. Сочетание газовой хроматографии с масс-спектрометрией дает метод, с помощью которого все компоненты сложной трехсоткомпонентной смеси можно разделить и идентифицировать, если даже их содержание в пробе составляет около 10-12г. Несмотря на впечатляющие возможности, физические принципы обоих методов достаточно просты.
Хромато-масс-спектрометрия является гибридным методом анализа, по этой причине должен рассматриваться как сочетание хроматографии (газовой или жидкостной) и масс-спектрометрии. Процессы разделения и анализа здесь протекают совершенно независимо друг от друга.
В 1952 г. английский ученый А. Дж. Мартин и его сотрудник А. Джеймс, занимаясь анализом жирных кислот, сделали два очень важных наблюдения. Во-первых, они обнаружили, что методом хроматографии можно разделить не только растворенные жидкие вещества, но также газы и пары. Во-вторых, они показали, что разделение может осуществляться не только благодаря многократному повторению цикла адсорбция-десорбция, но и путем чередования абсорбции и десорбции.
Слова адсорбция и абсорбция отличаются между собой одной буквой, но используются они для обозначения совершенно различных процессов. Адсорбция представляет собой концентрирование вещества на поверхности раздела фаз (твердой-газообразной, твердой- парообразной, твердой-жидкой). При абсорбции растворы, газы или пары тоже соприкасаются с жидкой фазой, но молекулы этих веществ не задерживаются на поверхности раздела, а поглощаются, то есть растворяются, в объеме жидкости и твердого тела (рис.1). Явления, связанные с абсорбцией газов в жидкостях, лежат в основе газожидкостной хроматографии наиболее распространенного в настоящее время метода разделения. Когда над жидким раствором находится газ, то между молекулами газа, которые растворяются в жидкости, в теми, что остаются в газовой фазе, устанавливается динамическое равновесие. Если над жидкостью находится не индивидуальный газ, а смесь газов и эта смесь начнет перемещаться, то отдельные компоненты газовой смеси, обладая различной растворимостью в этой жидкости, передвигаются с разными скоростями. В конечном счете газовая смесь разделится на составные части. Как видно, принцип разделения жидких смесей, предложенный Цветом, может найти применение и для анализа смесей газов. Внедрение этого принципа в аналитическую практику открыло «золотой век» хроматографии, который продолжается и в наши дни.

Большинство хроматографических методов основано на том, что анализируемую смесь вместе с подвижной фазой пропускают через хроматографическую колонку. В зависимости от того, является ли неподвижная фаза твердым носителем или жидкостью, компоненты анализируемой смеси адсорбируются на поверхности твердого тела или растворяются в жидкости. В результате эти компоненты удерживаются неподвижной фазой и продвигаются по колонке медленнее, чем инертная подвижная фаза. Если условия хроматографирования благоприятны для разделения, то каждый компонент удерживается неподвижной фазой по-разному. В результате скорости продвижения отдельных компонентов вдоль колонки будут неодинаковы, и, как и в опытах Цвета, каждый компонент образует свое «кольцо», и эти «кольца», или, как их называют, зоны, раздельно, одна за другой выйдут из колонки.
Механизм разделения смесей в колонке не зависит от того, находятся ли отдельные компоненты в газовой фазе или в жидком растворе, хотя хроматографы, предназначенные для манипулирования с газами и жидкостями, имеют разную конструкцию. Прибор для анализа смесей в виде газа или пара называется газовым хроматографом, а метод анализа — газовой хроматографией. Жидкие смеси анализируют с помощью жидкостного хроматографа, и метод анализа получил название жидкостной хроматографии.
Все хроматографы имеют четыре основных части: устройство ввода пробы, хроматографическая колонка, детектор, регистратор. Принципиальная схема газового хроматографа приведена на рис. 2.
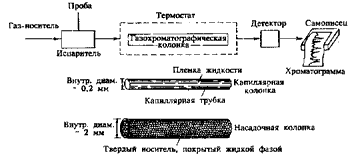
Колонку, в которой происходит разделение смесей, по праву считают «душой хроматографа», хотя в современных приборах это устройство совсем непохоже на широкую трубку, использованную Цветом в своих первых опытах. Как правило, хроматографические колонки изготовляют из металлических или стеклянных, а сейчас и кварцевых трубок, внутренний диаметр которых не превышает 2мм, длина меняется от нескольких сантиметров до нескольких метров. Для того чтобы длинные трубки можно было бы поместить в камеру хроматографа с регулируемой температурой, то есть в термостат, их обычно скручивают в спираль. В таких колонках находится неподвижная фаза. Твердая неподвижная фаза представляет собой пористый адсорбент. Колонки с жидкой неподвижной фазой можно приготовить двумя способами. Первый способ заключается в том, что в колонку помещают твердый адсорбент, предварительно пропитанный жидкой фазой. Второй способ состоит в том, что жидкую фазу наносят на стенки длинных капилляров.
Важной деталью хроматографа является дозатор-устройство для ввода пробы, которое позволяет быстро в виде компактной порции ввести в поток газа-носителя строго определенное количество анализируемого вещества. Очень часто пробу вводят следующим образом. Сначала образец набирают в шприц-дозатор иглой медицинского шприца, а затем, как показано на рис. 3, этой иглой прокалывают силиконовую прокладку и вводят соответствующий объем образца в поток газа-носителя. Другой широко распространенный метод введения пробы заключается в следующем. Вначале поток исследуемого газа пропускают через небольшую трубку, объем которой предварительно был точно определен. Затем поворотом крана в этот известный объем поступает газ-носитель и выталкивает оттуда в колонку оставшуюся пробу. Дозатор газового хроматографа снабжен обогревающим устройством, и это дает возможность подавать в прибор жидкие при комнатной температуре пробы. Обогреваемый дозатор очень быстро испаряет жидкую пробу, и образовавшиеся пары попадают в поток газа-носителя и вместе с газом поступают в разделительную колонку хроматографа.

Для того, чтобы проследить за процессом разделения, надо точно измерить время прохождения данного компонента смеси через колонку, то есть время выхода из колонки. Этой цели служит детектор-устройство, способное давать электрический сигнал при изменении какого-либо физического свойства компонентов, выходящих из колонки. Если через детектор проходит газ-носитель, на диаграммной ленте записывается более или менее горизонтальная прямая, которую называют нулевой линией. Если же с потоком газа-носителя в детектор попадает определяемый компонент с иными, чем у газа-носителя, физическими свойствами, перо самописца начнет отклоняться от нулевой линии и перемещаться в направлении, перпендикулярном направлению движения диаграммной ленты. После прохождения через детектор разделяемой на компоненты смеси, хроматограмма (запись на диаграммной ленте) представляет собой набор колоколообразных пиков, каждый пик соответствует, как правило, одному компоненту (рис. 4).

Детектор способен регистрировать изменение какого-то определенного физического свойства смеси, например ее теплопроводности или показателя преломления. Поскольку физические свойства выходящей из колонки смеси зависят от состава, момент прохождения через детектор отдельной зоны регистрируется соответствующим сигналом. Для идентификации органических веществ используется так называемое время удерживания, то есть время, прошедшее с момента введения пробы в хроматограф до момента появления вещества в детекторе (рис. 5).

Для большей надежности правильность идентификации проверяют с помощью чистого индивидуального соединения. Делается это следующим образом. Исследуемую смесь разбивают на несколько образцов и в каждый образец вводят строго определенное количество индивидуального соединения, присутствие которого предполагается в этой смеси. Если идентификация по времени удерживания проведена правильно, то высота соответствующего пика на хроматограмме после введения индивидуального соединения должна увеличиться. Однако этот метод нельзя назвать однозначным, потому что среди огромного количества органических соединений есть множество веществ с одинаковыми временами удерживания.
Начало масс-спектрометрии было положено работами физиков в 1908 г. К 1918 г. развитие метода достигло такой степени, что с его помощью было продемонстрировано существование у неона двух изотопов с массами 20 и 22. Эта информация привела к пересмотру концепций химических атомных масс и явилась предвестником атомной эры. К 1942 г. масс-спектрометры выпускались серийно для проведения анализа газовых смесей с большой скоростью и точностью. В настоящее время масс-спектрометрия относится к одной из главных дисциплин во всех аспектах научных исследований.
Масс-спектрометрию можно рассматривать как совокупность двух отдельных процессов: ионизации и разделения ионов по массам и регистрации образующихся ионов. Многочисленные методы ионизации можно сочетать с различными способами разделения ионов в зависимости от поставленных задач. На рис. 6 поясняется принцип действия магнитного масс-спектрометра.

При бомбардировке электронами молекул в газообразном состоянии связи в молекулах разрываются и образуются ионы. Вид и количество образующихся фрагментов характерны для данной молекулы. При наложении магнитного поля, положительно заряженные частицы ускоряются и движутся по изогнутым кривым, радиус кривизны которых пропорционален корню квадратному из массы иона. При некотором постоянном магнитном поле поток ионов, содержащий ионы с идентичным отношением масса/заряд, попадает на коллектор. Здесь при разряде ионов возникает ток, пропорциональный относительному количеству ионов с соответствующей массой. Изменением магнитного поля постепенно переводят на коллектор потоки ионов с другим отношением масса/заряд. Ток коллектора записывается и дает масс-спектрограмму. Масс-спектр может служить для идентификации молекулы.
В квадрупольном масс-спектрометре (рис. 7) разделение по массе достигается иным образом. Между четырьмя параллельными стержнями создается высокочастотное электрическое поле.

Когда пучок ионов попадает в это поле, только ионы с определенным отношением масса/заряд имеют стабильную траекторию и попадают на детектор (коллектор). Детектирование пучков с различным отношением масса/заряд (развертку масс-спектра) проводят варьированием параметров электрического поля.
Можно представить себе, с какими трудностями придется столкнуться, при попытке расшифровать масс-спектр образца, состоящего из нескольких веществ с большими молекулярными массами. В то же время, если подключить к масс-спектрометру газовый хроматограф, то интерпретировать спектры станет значительно легче, так как перед бомбардировкой смесь будет разделена на индивидуальные компоненты.
Уже давно масс-спектрометр рассматривают как отличный детектор для газовой хроматографии. Как газовый хроматограф, так и масс- спектрометр представляют собой в принципе относительно несложные приборы, а получаемые с помощью каждого из них аналитические данные просты для понимания и использования. Когда эти два прибора напрямую соединяют в единую
хромато-масс-спектрометрическую систему, возможности такой системы не равны просто сумме возможностей каждого прибора; аналитические возможности увеличиваются экспоненциально. Для того, чтобы реализовать весь потенциал, заключенный в громадном количестве данных, генерируемых хромато-масс-спектрометром, необходим специализированный компьютер. С подключением компьютера к прибору становятся возможными многие операции с данными, увеличивающие их аналитическую ценность. Полученные с помощью масс-спектрометрического детектора спектры, дают такую информацию о качественном составе пробы, какую не могут дать иные газохроматографические детекторы. Масс-спектрометрический детектор обладает большей чувствительностью, кроме того, он разрушает пробу, дает информацию о массе и различает скорее гомологи, чем изомеры.
Принципиальная схема масс-спектрометра в комбинации с газовым хроматографом представлена на рис. 8.

Первым шагом при хромато-масс-спектрометрическом анализе является обычно сканирование по всему диапазону масс (рис. 9). Идентификацию проводят с помощью библиотеки спектров, чаще всего заложенной в память ЭВМ, которая одновременно и управляет работой детектора. Изучение характеристических пиков и молекулярных ионов играет важную роль при идентификации соединения.

Следующим шагом является качественный анализ, для чего используют метод регистрации отдельных ионов (SIM). Для этого применяют фильтр, чтобы исследовать только несколько видов ионов и тем самым повысить чувствительность.
Наконец, суммируют все осциллограммы по отдельным ионам и наносят на диаграмму с единым масштабом времени (рис. 10), чтобы получить хроматограмму по всем ионам в пробе (TIC).

Дальнейшее развитие ГХ/МС-методов и широкое применение компьютерной техники привело к тому, что масс-спектрометрия стала доступной не только специалистам, но активно используется в качестве стандартного метода детектирования в газовой хроматографии. Компьютер управляет системой в целом, записывает данные, накапливает массовые спектры. Накопление большого количества масс-спектров за секунду требует большого объема памяти и высокого быстродействия машины.
Пример применения хромато-масс-спектрометрии для разделения смеси лекарственных веществ приведен на рис. 11.

Сравнение спектра вещества с временем удерживания морфина (рис.11) и сравнение со спектром морфина, заложенным в банк данных (рис.12).

В наши дни масс-спектрометры выпускают только в комплекте с компьютером. Большую помощь при идентификации оказывает банк масс-спектральных данных, который заказчик получает вместе с прибором. По мере выполнения масс-спектрометрических анализов новые результаты непрерывно вводятся в память компьютера, пополняя банк данных. При необходимости воспользоваться банком аналитик посылает в ЭВМ запрос, и компьютер сам находит в памяти спектр, который лучше других соответствует регистрируемому в данный момент спектру. Оба спектра появляются на экране, и теперь остается только сопоставить две спектральные картины. Сравнение спектров, то есть своеобразное опознание по «отпечаткам пальцев», значительно проще для идентификации неизвестных веществ, чем реконструкция молекул по отдельным фрагментам. Единственное необходимое условие для такой идентификация-наличие в банке данных спектра того самого вещества, которое поступило для анализа.
Хромато-масс-спектрометрия нашла широкое применение в различных областях химии, медицины, фармацевтического производства, экологического мониторинга и технологического контроля в промышленности.
| ЖУРНАЛ | ЛАБОРАТОРИИ | ЛИТЕРАТУРА | ОБОРУДОВАНИЕ | РАБОТА | КАЛЕНДАРЬ | ФОРУМ |
| Copyright © 2002-2022 «Аналитика-Мир профессионалов» |
Размещение рекламы / Контакты |